
今回は、「質量保存の法則」について説明します。
中学生で学習する化学の範囲の中で、そのメインに位置すると言えるのが、いわゆる「化学反応式」の分野です。
化学反応式を学習する際には、いくつもの化学反応や化学式を暗記しなければなりません。
その数は多いですし、化学反応式を作り上げる時には、複雑な係数処理をしなければならないことから、中学化学の学習をする場合には、どうしてもこれらの分野に時間を取られてしまいがちです。
ただし、化学反応式について、なぜこれらの反応式が成立するのかを考えたとき、その前提には「質量保存の法則」が常に存在しているということを忘れてはいけません。
化学反応式の前提にあるのが「質量保存の法則」
反応の前後で質量がかわらないから、反応前後についての関係式を作り上げることができるわけですし、また、それが問われるのです。
したがって、化学反応式等に関する細かい知識に気を取られてしまうのは仕方のないことですが、ふとしたタイミングでこの前提に立ち返ることで、理解を再び積み上げ、頭の中で知識を整理するための良い機会としてはいかがでしょうか?
そのための「質量保存の法則」について、今回は説明をしていきたいと思います。
質量保存の法則
質量保存の法則とは
化学変化の前後で、物質全体の質量はかわりません。この性質を質量保存の法則と言います。
例えば、気体が発生する化学反応や、空気中の酸素と化合する化学反応も、密閉された容器内で行われた場合には、反応の前後で物質全体の質量はかわりません。
逆の言い方をすれば、気体が発生する化学反応において、発生した気体が外に逃げてしまうと、物質全体の質量は減少します。
石灰石と塩酸
石灰石に塩酸をかけると、これらが化学変化を起こし、塩化カルシウムと水と二酸化炭素が発生します。
これらの化学反応が密閉された空間内で行われた場合には全体の質量に変化はありませんが、発生した二酸化炭素が密閉空間から漏れでた場合には、全体の質量が減少することになります。
また、空気中の酸素と化合する化学反応において、この化学反応が密閉された空間内で行われない場合には、化合した酸素分の質量分、全体の質量が増加することになります。
銅の燃焼
銅を燃焼すると、銅が空気中の酸素と結び付くことによって酸化銅が生成されます。
この時、これら一連の作業が密閉した空間内で行われた場合には物質全体の質量に変化はありませんが、そうでない場合には、銅と化合した酸素の質量分、物質全体の質量が増加することになります。
質量保存の法則のイメージを掴むために
教科書的な具体例を挙げることもできますが、その前に質量保存の法則についてイメージを掴みやすい良い例を一つ提示しておきます。
質量保存の法則を発見したのはフランス人科学者のラボアジエです(覚えておくと良いでしょう)。その彼が行った実験が非常にわかり易いものとなっています。
密閉したフラスコを100日間加熱し続けた実験
彼は、フラスコの中に水を入れ、そのフラスコに蓋をして完全に密閉しました。
そして、水の入ったこのフラスコを100日間加熱し続けたのです。100日もの間これを加熱したのですから、当然中の水は完全になくなってしまいますし、さらに、フラスコの形状も変形をしてしましました。
にもかかわらず、加熱前のフラスコ全体の質量と、100日間加熱した後のフラスコ全体の質量に変化はありませんでした。
これはまさに質量保存の法則の典型例と言えるでしょう。
質量保存の法則の豆知識
質量保存の法則を一生懸命学習しようとしている学生に対して次のことを述べるのは気がひけてしまうのですが、実は、「質量保存の法則」は現在では公理としては認められていないのです。
かの有名なアインシュタインが相対性理論を提唱したことは有名でしょう。
この相対性理論の有用性が確立されたことによって、それまで確立していたと考えられていたいくつもの公理が影響を受けましたが、今回説明している質量保存の法則もその一例なのです。
興味がある方は相対性理論についての簡単な説明について調べてみて下さい。現在では、質量保存の法則は、相対性理論に後れるものとされていることが分かると思います。
それではなぜ質量保存の法則を学習する必要があるのでしょうか。
質量保存の法則を学ぶ意義
実は、厳密な原理的な部分では、相対性理論の方が質量保存の法則よりも正確性の高い説明をすることができるというだけで、相対性理論によって導かれる結論に対して、質量保存の法則もほとんど近似的な結論を得ることができることから、実用的な意味では、今なお質量保存の法則の利用価値はあるとされているのです。
目盛りが剥げて見えにくくなった定規でも、直線を引く上では有効である、というようなものでしょう。
したがって、私たちはまず、質量保存の法則についてしっかりと学習しなければならないのです。
そして、高校、大学と、学問に深みを増す段階になったときに、実は学問的な観点からは質量保存の法則は正確なものではないのだ、ということを理解することが、学習段階の一つに位置付けられているというわけです。
グラフ問題の解き方
さてここからは実際の問題を解いてみましょう。
質量保存の法則が成立する前提ですが、物質同士が化合する場合、その「質量の比」は常に一定という性質が導かれます。
マグネシウムを燃焼させる
例えば、マグネシウムを燃焼すると酸化マグネシウムを生成することができます。
マグネシウム+酸素→酸化マグネシウム
2Mg+O₂→2MgO
化学反応式はこの通りですが、ここで少し注意しなければならないことがあります。
化学反応式は「分子の比」であり「質量の比」ではない
この化学反応式をしっかりと読解すると、「2つのマグネシウム分子と1つの酸素分子によって、2つの酸化マグネシウム分子ができる」となります。
つまり、ここから読み取ることができるのは、「分子の数の比」で、「質量の比」を読み取ることができるわけではないということです。
したがって、しばしば勘違いをしてしまう生徒がいるのですが、化学反応式の係数の比に注目できる姿勢は正しいことなのですが、それはあくまでも「分子数の比」を表現したものであり、「質量比」ではないということを忘れないようにしましょう。
質量比はそれぞれの分子の質量(重さ)を考慮に入れて検討しなければいけません(そして、その詳細な計算については高校生の範囲ですので、今のところはその算出方法について理解する必要はありません)。
「質量の比」をグラフから読み取る
中学生で出題されるのは以下のようなグラフです。
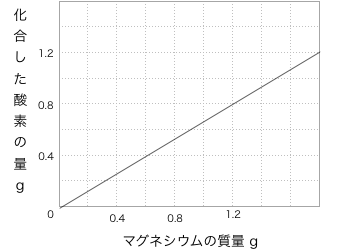
このようなグラフから、マグネシウムと酸素の質量比について考えるのです。つまり、マグネシウム1.2gに対して、これと化合するための酸素は0.8gであることを読み取ることができますね。したがって、ここに、マグネシウムと酸素の質量比は
1.2:0.8=3:2
と導くことができるでしょう。
そして、化合する物質の質量比が一定であるという性質から、他のマグネシウムの質量に対応する、化合に要する酸素質量を求めることもできるようになります。
例えば、マグネシウムの質量が0.9gのとき、マグネシウムと酸素の質量比が3:2であることから、3:2=0.9:0.6より、化合に必要な酸素の質量は0.6gであることを導くことができます。
さらに、この場合について、質量保存の法則を直接的に利用することによって、生成された酸化マグネシウムの質量について、0.6g+0.9g=1.5gと導くこともできます。
グラフをしっかり読解できるように
このグラフを読み解く問題は、案外出題される形式ですので、しっかりと練習しましょう。
また、今回は「横軸にマグネシウム、縦軸に酸素」というグラフが提示されましたが、場合によっては、「横軸にマグネシウム、縦軸に酸化マグネシウム」というグラフが出題されることもありますので、グラフを注意深く観察する必要があります。
数学の成績にも直結する部分ですので、おろそかにしないようにしましょう。
質量保存の法則についての問題
質量保存の法則に関連するものとして、「発生する気体の体積は、反応した物質の質量に比例する」という性質が挙げられます。塩酸にマグネシウムを入れる場合について考えてみましょう。
塩化マグネシウムを生成する
塩酸にマグネシウムを入れると、塩化マグネシウムが生成され、水素が発生します。化学反応式の作り方は化学反応式はこれで完璧を参照してください。
塩酸+マグネシウム→塩化マグネシウム+水素
2HCl+Mg→MgCl₂+H₂
さて、この反応について、発生する気体である水素について注目したとき、その質量はマグネシウムの質量に比例することになるのです。マグネシウムが多ければ多いほど、発生する水素の質量も増加することになります。ただし、これについても注意が必要です。
ある時点からは水素が発生しない
マグネシウムをどれだけ増やしたとしても、塩酸の量が一定であれば、ある時点において全ての塩酸がマグネシウムと反応しきってしまう点が訪れることになります。
この段階に達すると、それ以上水素が発生することもありませんし、したがって、マグネシウムの質量に対応する形で水素の質量も増加するという関係ではなくなることになります。
つまり、ある時点までは両者は比例するが、液体と全て反応した場合には、それ以後比例の関係ではなくなる、ということになります。
以上で説明したことをグラフにするとこのようになります。
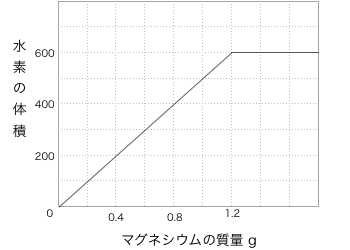
この図より、マグネシウムが1.2gまでは、塩酸と反応することによって水素が発生していましたが、マグネシウムと反応できる塩酸がこの時点でなくなってしまったことになります。
したがって、これ以降は、マグネシウムの質量をどれだけ増やしたとしても、発生した水素の質量に変化はありません。このグラフもよく出題されるのでしっかりと読解できるようにしましょう。
さいごに
実はグラフ問題が出題されることが多い分野でもあります。しかも、化学反応式が密接に絡んでくる範囲ですから、どうしても化学反応式における係数とリンクさせようと体が反応してしまいがちです。
勤勉な生徒ほど、質量比と化学反応式について混同してしまう場合がありますし、出題者はそこの間隙を狙ってあえてこの分野を出題することが考えられます。
簡単な分野ではありますが、基本を大切に、丁寧な理解を心掛けましょう。